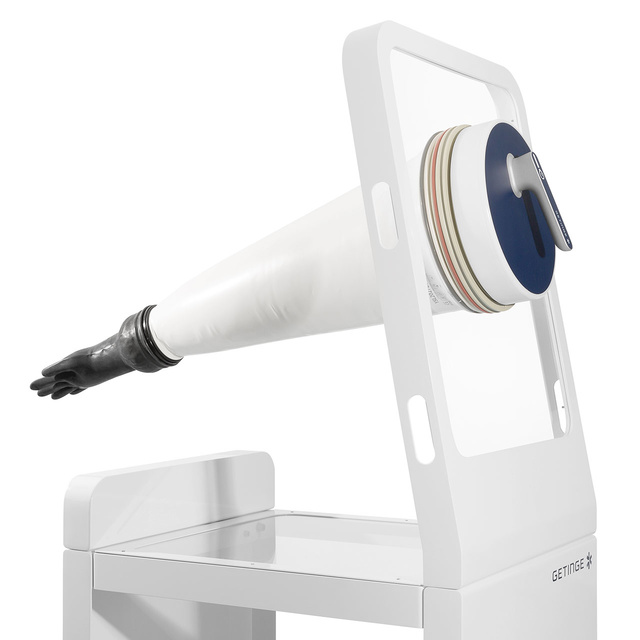
Das DPTE® Transfer-Leckagetestgerät (TLT) gewährleistet Compliance und Integrität
Kabel- und schlauchlose Prüfungen an DPTE® Alpha- und Beta-Teilen
Erfüllen Sie alle aktuellen und zukünftigen Vorschriften
Wir wissen, dass Sie die ständig steigenden Anforderungen an die Prüfung der Prozessintegrität unter Druck setzen. Der neue Anhang 1 des EU-Leitfadens zur Guten Herstellungspraxis trägt ebenfalls seinen Teil dazu bei. Das überarbeitete, kabellose Getinge TLT wurde entwickelt, um diese Anforderungen zu erfüllen und die Überprüfung der Integrität von DPTE® Alpha- und Beta-Teilen weiterhin einfach und komfortabel zu gestalten. Für die Prüfung wird Druck mit zuverlässiger und genauer Wiederholbarkeit verwendet.
Das Getinge TLT - Hier kommen Sie zum Produktvideo: TLT- Transfer-Leckagetestgerät
Das neue bedienerfreundliche TLT ermöglicht Ihnen die Überprüfung der Integrität der DPTE®-Systeme vor oder nach den Produktionszyklen beim geschlossenen Transfer von Materialien in oder aus Isolatoren oder anderen klassifizierten Umgebungen sowie bei der Lagerung aseptischer Behälter zwischen Prozessen.
Weitere Informationen zu sterilen Transfersystemen auf unserer Webseite: Aseptischer Transfer
* Europäische Kommission, EudraLex, Band 4, EU Leitlinien für die Gute Herstellungspraxis Humanarzneimittel und Tierarzneimittel,
Anhang 1, Herstellung steriler Arzneimittel, Dezember 2017 (Entwurf zur Stellungnahme).
FDA Aseptic Processing Guidance
PIC/S Pharma Inspection Convention Cooperation Scheme, Section 9.5.3